El hidrógeno es el primer elemento químico de la tabla periodica. El hidrógeno es el elemento químico de número atómico 1, representado por el símbolo H. Tiene únicamente un protón en el núcleo y un electrón dando vueltas sobre él.
El hidrógeno es el elemento químico más abundante, constituyendo aprox. el 75 % de la materia visible del universo. Por ejemplo, las estrellas están compuestas principalmente por hidrógeno en estado de plasma. En la Tierra forma parte de las moléculas de agua, de todos los ácidos e hidrocarburos. Sin embargo como elemento aislado es relativamente raro y se produce a partir de hidrocarburos. La mayor parte del hidrógeno elemental se consigue en el lugar y en el momento en que se necesita.
Indice
PROPIEDADES FÍSICO-QUIMICAS DEL HIDRÓGENO
Masa atómica: 1,00794 u ± 0,00001 u
Densidad: 0,0899 kg/m3
Radio atómico (calc): 53 pm (radio de Bohr)
Grupo, período, bloque: 1, 1, s
Nombre, símbolo, número: Hidrógeno, H, 1
Estado ordinario: Gas
Punto de fusión: 14,025 K (-259 °C)
Punto de ebullición: 20,268 K (-253 °C)
Calor específico: 1,4304·104 J/(K·kg)
nºCAS: 1333-74-0
nº EINECS: 215-605-7
ESTRUCTURA ATÓMICA DEL HIDRÓGENO E ISÓTOPOS
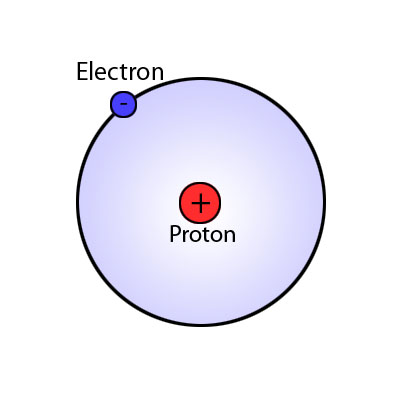 El átomo de hidrógeno tiene 2 isótopos: El segundo isótopo se llama deuterio y tiene un núcleo formado por un protón y un neutrón, es un isótopo estable pero poco abundante en la naturaleza (sólo un 0,015% de los átomos de hidrógeno son de deuterio). El tercer isótopo, llamado tritio tiene un núcleo formado por dos neutrones y un protón, debido al desequilibrio entre protones y neutrones este átomo es inestable y se desintegra radiactivamente dando lugar a un átomo de Helio:
El átomo de hidrógeno tiene 2 isótopos: El segundo isótopo se llama deuterio y tiene un núcleo formado por un protón y un neutrón, es un isótopo estable pero poco abundante en la naturaleza (sólo un 0,015% de los átomos de hidrógeno son de deuterio). El tercer isótopo, llamado tritio tiene un núcleo formado por dos neutrones y un protón, debido al desequilibrio entre protones y neutrones este átomo es inestable y se desintegra radiactivamente dando lugar a un átomo de Helio:
EL HIDRÓGENO EN LA NATURALEZA
El hidrógeno es el elemento químico más abundante en la naturaleza, constituye aproximadamente el 75% de la materia visible del universo. Tanto las estrellas como el sol están compuestas principalmente por hidrógeno en estado de plasma. El hidrógeno elemental es relativamente raro en la Tierra, se obtiene in situ en el momento que se necesita, normalmente a partir de hidrocarburos.
El hidrógeno forma compuestos con la mayoría de los elementos químicos. Está presente en el agua (H2O) y en la mayoría de los compuestos orgánicos. Tiene un papel particularmente importante en la química de las reacciones ácido-base y en el pH de las disoluciones. Las reacciones ácido-base que implican un intercambio de iones H+ entre las moléculas. El estudio de la energía y del enlace del átomo de hidrógeno ha sido fundamental hasta el punto de haber desempeñado un papel principal en el desarrollo de la mecánica cuántica.
INFLAMABILIDAD
El gas H2 (dihidrógeno) es altamente inflamable y se quema en concentraciones de 4 % o más H2 en el aire. La entalpía de combustión de hidrógeno es −286 kJ/mol; se quema de acuerdo con la siguiente ecuación balanceada.
- 2 H2(g) + O2(g) → 2 H2O(l) + 572 kJ (286 kJ/mol)
COMPUESTOS Y APLICACIONES DEL HIDRÓGENO
COMPUESTOS ORGÁNICOS
El hidrógeno forma una enorme variedad de compuestos con el carbono. Debido a su presencia en los seres vivos, estos compuestos se denominan compuestos orgánicos; sus propiedades forma parte de la química orgánica.
El enlace carbono-hidrógeno, CH, es el que proporciona a estos compuestos muchas de sus principales características. Las clases de compuestos que sólo poseen enlace carbono-hidrógeno C-H y enlaces carbono-carbono C-C se llaman hidrocarburos. El enlace C-H es difícil de romper. El tipo de reacciones en que se destruyen estos enlaces requieren un aporte de energía para iniciar la reacción, como por ejemplo: Combustiones, sustituciones, reacciones ácido-base.
COMPUESTOS INORGÁNICOS
Algunos ejemplos de compuestos covalentes importantes que contienen hidrógeno son: amoniaco (NH3), hidracina (N2H4), agua (H2O), peróxido de hidrógeno (H2O2), sulfuro de hidrógeno (H2S), etc.
HIDRUROS
A menudo se denomina hidruro a cualquier compuesto del hidrógeno, pero esto es muy inexacto. El término hidruro implica que el átomo de hidrógeno ha adquirido carga parcial negativa ( H–).
ÁCIDOS
La oxidación del H2 origina el protón, H+. Un protón aislado H+ no puede existir en disolución debido a su fuerte tendencia a unirse a átomos o moléculas. Para evitar la cómoda, aunque incierta, idea del protón aislado en disolución, en las disoluciones ácidas acuosas se considera la presencia del ion hidronio (H3O+). Algunos ácidos más conocidos son el ácido clorhídrico, ácido sulfúrico,…
ENERGÍA DEL HIDRÓGENO
El hidrógeno no es una fuente de energía, únicamente se encuentran en desarollo (pero lejano de ser realidad) la fusión de deuterio o tritio.
La energía del sol proviene de la fusión nuclear del hidrógeno, pero este proceso es difícil de lograr de forma controlable en la Tierra. El hidrógeno elemental de fuentes solares, biológicas, o eléctricas requieren más energía para crear lo que es obtenido al quemarlo, por lo que, en estos casos, sirve el hidrógeno como portador de energía, como una batería. Se puede obtener a partir de fuentes fósiles (tales como metano), pero estas fuentes son insustentables.
APLICACIONES DEL GAS H2
- Mejoramiento de combustibles fósiles
- Producción de amoníaco.
- El H2 se utiliza como un agente hidrogenizante, particularmente en el aumento del nivel de saturación de las grasas y aceites insaturados (que se encuentran en artículos como la margarina)
- Producción de metanol.
- Agente reductor de minerales metálicos.
- H2 líquido se utiliza en la investigaciones criogénicas, incluyendo estudios de superconductividad.
- Dado que el H2 es más ligero que el aire, teniendo un poco más de 1/15 de la densidad del aire, fue ampliamente utilizado en el pasado como gas de elevación en globos aerostáticos y dirigibles.
- Es un aditivo alimentario autorizado (E 949) que permite la prueba de fugas de paquetes, entre otras propiedades antioxidantes.
EXPERIMENTOS RELACIONADOS CON EL HIDRÓGENO
Dado que está presente en los ácidos, cualquier experimento relacionado con el pH o con reacciones ácido-base, serían experimentos en los que interviene el hidrógeno. Aquí puedes ver el listado de todos los experimentos. Hay un experimento en concreto en el que producimos gas hidrógeno a partir de ácido clorhídrico y metal:
Experimento Producir Hidrógeno, H2, a partir de Aluminio y Ácido Clorhídrico