El átomo está compuesto por un núcleo de protones (cargados positivamente) y neutrones y electrones (cargados negativamente) que circulan en órbitas alrededor del núcleo. Los electrones son los responsables de los enlaces químicos que se producen entre los átomos. Su distribución y número de electrones en la última capa son fundamentales de cara a establecer los diferentes enlaces que se pueden establecer.
Indice
DISTRIBUCIÓN ELECTRONES EN LOS ÁTOMOS
Los electrones no circulan libremente alrededor del núcleo, sino que lo hacen en determinados niveles de energía, en diferentes capas. Según el número de electrones que tenga cada elemento (igual al número de protones, se puede ver en la tabla periódica, a través del número atómico, el número de protones de cada elemento), se irán completando niveles de energía.
Un elemento será cuanto más estable cuanto más completo tenga el último nivel de energía. Así mismo el número de electrones que le falten o sobren para completar la última capa es lo que nos va a dar el número de oxidación de cada elemento y la tendencia que va a tener a combinarse con otros elementos a través de los enlaces químicos.
CAPAS O NIVELES DE ENERGÍA DE LOS ELECTRONES
Los diferentes niveles pueden albergar diferente número de electrones . Este es:
| s | p | d | f | |
|---|---|---|---|---|
La forma de ir completando estos niveles de energía se puede sacar por la siguiente regla de Aufbau:
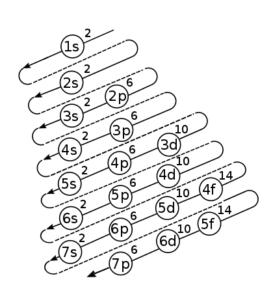
Es decir, primero se completará en nivel 1 con 2 electrones: 1s2, después el nivel 2: 2s2, después 2p6 3s2, después 3p6 4s2, siguiente nivel 3d10 4p6 5s2
Así sucesivamente hasta llegar a la configuración completa de electrones que es:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p6
Para determinar la configuración electrónica de un elemento, basta con calcular cuántos electrones hay que acomodar y entonces distribuirlos en los subniveles empezando por los de menor energía e ir llenando hasta que todos los electrones estén distribuidos. Un elemento con número atómico mayor tiene un electrón más que el elemento que lo precede. El subnivel de energía aumenta de esta manera:
ELECTRÓN DE VALENCIA
Los electrones de valencia son los electrones que se encuentran en la capa de mayor nivel de energía o última capa del átomo. Son los responsables de los enlaces entre átomos de distintos elementos o entre los átomos de un mismo elemento. Los electrones de valencia son los que serán utilizados en la formación de compuestos.
VALENCIA O NÚMERO DE OXIDACIÓN
El número de electrones que faltan o sobran para completar la última capa se le llama valencia o número de oxidación. Aquí algunas reglas:
- El estado de oxidación de todos los elementos en estado libre, no combinados con otros, es de cero (p. ej., Na, Cu, Mg, H2, O2, Cl2, N2).
- El estado de oxidación del H es de +1, excepto en los hidruros metálicos, en los que es de -1 (p. ej., NaH, CaH2).
- El estado de oxidación del O es de -2, excepto en los peróxidos, en los que es de -1, en los superóxidos que es -1/2 y en el OF2, donde es de +2.
- El estado de oxidación del elemento metálico de un compuesto iónico es positivo.
- En los compuestos covalentes, el número de oxidación negativo se asigna al átomo más electronegativo y todos los demás son positivos.
- La suma algebraica de los estados de oxidación de los elementos de un compuesto es cero.
- La suma algebraica de los estados de oxidación de los elementos de un ion poliatómico es igual a la carga del ion.1
REGLA DEL OCTETO
La regla del octeto define la propiedad que tienen los átomos de completar su último nivel de energía con ocho electrones para alcanzar estabilidad. Ya sea un enlace iónico, covalente o metálico, los átomos van a tender a ceder o compartir para completar 8 electrones en la capa de valencia. Ver más información sobre la regla del octeto.
Interesante